糖化血红蛋白
 血红蛋白A1是主要的糖化血红蛋白成分,正常情况下体内糖化血红蛋白约占血红蛋白总量6%~8%,无性别、年龄、种族的差别。当糖尿病时糖化血红蛋白较正常人高2~3倍。且与过去的2~3个月间的空腹血糖水平密切相关。血糖浓度越高,糖化血红蛋白的相对百分率越高。糖化血红蛋白在糖尿病病程中下降缓慢。在糖尿病被控制和血糖浓度下降的患者糖化血红蛋白仍升高,故测定糖化血红蛋白能反映出患者过去2~3个月的血糖平均水平,但不能反映近期的血糖水平。糖化血红蛋白测定用于评价糖尿病的治疗控制程度。
血红蛋白A1是主要的糖化血红蛋白成分,正常情况下体内糖化血红蛋白约占血红蛋白总量6%~8%,无性别、年龄、种族的差别。当糖尿病时糖化血红蛋白较正常人高2~3倍。且与过去的2~3个月间的空腹血糖水平密切相关。血糖浓度越高,糖化血红蛋白的相对百分率越高。糖化血红蛋白在糖尿病病程中下降缓慢。在糖尿病被控制和血糖浓度下降的患者糖化血红蛋白仍升高,故测定糖化血红蛋白能反映出患者过去2~3个月的血糖平均水平,但不能反映近期的血糖水平。糖化血红蛋白测定用于评价糖尿病的治疗控制程度。
- 专科分类 生长发育检查
- 检查分类 血液检查
- 适用性别 男女均适用
- 是否空腹 空腹
- 参考价格 25元
研究历史
糖化血红蛋白于1958年被使用色谱法首次从其它类型的血红蛋白中分离出来,并于1968年被分类为一种糖蛋白。1969年,人们发现糖化血红蛋白在糖尿病患者中的数量增加。1975年研究者们得到了生成糖化血红蛋白的反应式。
 糖化血红蛋白
糖化血红蛋白 自从1968年第一次描述了在糖尿病患者中发现的异常血红蛋白以来,关于葡萄糖及其他碳水化合物与血红蛋白结合的糖化产物的术语,已经变化几次。自从1986年,IUPAC-IUB(国际纯化学与应用化学联合会)已经推荐使用糖化血红蛋白这一名称,即非酶促的血红蛋白的糖基化。另一方面,更高级的术语糖基化血红蛋白经常地用于日常语言和现在的出版物里。
根据每个糖化位点和反应参与物,总的糖化血红蛋白分成若干个亚组分。天然(非糖化)血红蛋白是A0(2α、2β链)。亚组分(HbA1a1 , HbA1a2 , HbA1b和HbA1c)因血红蛋白β链-N末端缬氨酸的游离氨基与不同碳水化合物糖基化而形成。这些亚组分总称为HbA1。除了血红蛋白β链的N末端缬氨酸外,血红蛋白分子内其他游离氨基也参与糖基化(α链N末端缬氨酸、赖氨酸ε-氨基)。
 糖化血红蛋白
糖化血红蛋白 相对于HbA1,所有β-链N末端和其他游离氨基糖基化的血红蛋白被称作总糖化血红蛋白。除基本的成人血红蛋白AO外,在健康人里发现少量的胎儿血红蛋白HbF(2α、2γ链)和血红蛋白A2(2α、2δ链)。缬氨酸在δ链N末端,以类似的方式糖基化,例如,通过与葡萄糖的共价键形成HbA2c。亲和层析测定的糖化血红蛋白作为总糖化血红蛋白。
与血糖区别
血糖是从食物中的碳水化合物分解而来的血液中的单糖,通常仅指葡萄糖。血糖测试结果反映的是即刻的血糖水平。糖化血红蛋白测试通常可以反映患者近8~12周的血糖控制情况。糖化血红蛋白是糖尿病诊断新标准和治疗监测的"金标准" 随着人们对糖尿病知识的逐步了解,多数人已意识到空腹和餐后2小时血糖监测的重要性,并常常把二者的测定值作为控制血糖的标准。其实不然,空腹和餐后2小时血糖是诊断糖尿病的标准,而衡量糖尿病控制水平的标准是糖化血红蛋白。空腹血糖和餐后血糖是反映某一具体时间的血糖水平,容易受到进食和糖代谢等相关因素的影响。糖化血红蛋白可以稳定可靠地反映出检测前120天内的平均血糖水平,且受抽血时间,是否空腹,是否使用胰岛素等因素干扰不大。因此,国际糖尿病联盟推出了新版的亚太糖尿病防治指南,明确规定糖化血红蛋白是国际公认的糖尿病监控"金标准"。如果空腹血糖或餐后血糖控制不好,糖化血红蛋白就不可能达标。
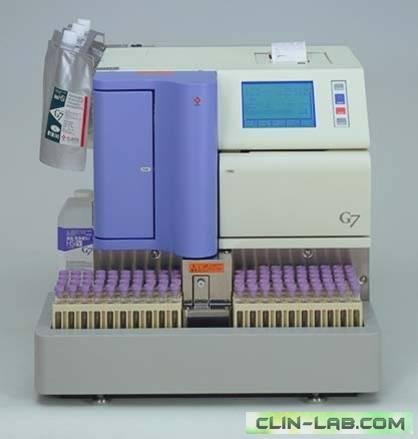 糖化血红蛋白仪
糖化血红蛋白仪
检测方法
1、阳离子交换色谱法
原理:糖化导致血红蛋白分子表面阳离子丢失。在弱的阳离子交换剂中,例如Biorex70,伴有增加的离子浓度和(或)pH下降,糖化血红蛋白在非糖化血红蛋白前先洗脱。这现象产生了糖化血红蛋白最初的术语"快速血红蛋白"。阳离子交换色谱法可用于小型、微型或大型柱层析方法或部分或全自动的PHLC/FPLC方法。因为,其他翻译后修饰血红蛋白,例如醛亚胺型、甲酰化、乙酰化、乙醛加合物、降解物、老化人工物品和异常血红蛋白电荷交换也不同于正常的HbA0,所以已经列出了许多阳离子交换层析法的干扰因素。使用常规HPLC的方法。分离糖化血红蛋白亚组分是能达到满足需求的临床精密度。然而,已知HbA1c的峰不是均一的而是包含一重要的非糖化血红蛋白部分。少数糖化血红蛋白也整合到HbA0主峰中。通过使用特殊的柱原料(poly-CATA)和30~40 min分离时间可以改善分离效果。这些方法可以作为参考步骤但不适合常规使用。所有的阳离子交换色谱法对pH和温度的变化敏感,因此要控制pH和温度。
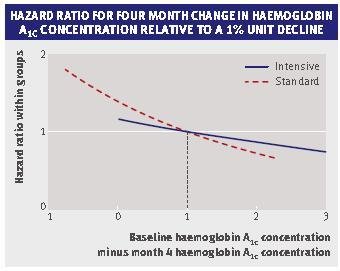
说明:根据红细胞代谢动力学推测初始HbA1c值大约每日破坏1/120(≈0.83%)。因为糖化在合适的治疗下甚至健康人也产生,故这个理论值在体外不能达到。控制不理想的糖尿病患者通过加强治疗而达到血糖量正常,可以发现HbA1c值最大下降率以大约每10 d下降正常血糖的1%(绝对的)。由于测定糖化血红蛋白方法的精确性,两次测定值HbA1c的差异大约1%就可认为具有临床相关性。因为这些原因,在HbA1c两次测定间至少有2周的时间,推荐4~6周的间隔。
因为升高的糖化血红蛋白值是长期高糖血症的糖尿病患者相当可靠的指示剂,因而是可能诊断糖尿病的。在未治疗的个体,正常的糖化血红蛋白值临床上可以排除明显的糖尿病。但由于它不能检测糖耐量受损,所以作为诊断和(或)筛选目的唯一的参数,使用糖化血红蛋白是存在问题的。
2、电泳法
原理:相比于非糖化血红蛋白,因糖化而变化的总电荷和糖化血红蛋白的等电点变化是琼脂糖凝胶或者pH梯度5.0~6.5的凝胶等电聚焦电泳分离的基础。琼脂糖凝胶电泳的血红蛋白亚组分分辨率很小,而等电聚焦可以更好地使亚组分分离。可能由于试验的自动化程度不足,重要性已经下降。
3、亲和层析法
原理:硼酸结合顺式-羟基。商品化的m-氨基苯硼酸琼脂糖共价结合的亲和柱已可用于微柱分析检测。将血样本中的血红蛋白加到层析柱后,所有的糖化血红蛋白(HbA1和旁链糖化的血红蛋白;总糖化血红蛋白)与硼酸结合而非糖化血红蛋白通过层析柱可被测量。在加入高浓度也包含顺式-羟基的多羟基复合物,例如山梨醇后,糖化血红蛋白与硼酸的结合被替换而从柱子上洗脱下来。亲和层析法对经翻译以后修饰的血红蛋白和病理血红蛋白的影响相对不敏感。利用亲和层析法,仅能测定总糖化血红蛋白。广泛使用的亲和层析方法,允许用经验算法从总糖化血红蛋白值计算出"标准的HbA1c"。
4、免疫分析法
在缬氨酸β-N-末端糖化的血红蛋白提供了一个容易被抗体识别的抗原表位。可以用单克隆抗体或多克隆抗体进行放射免疫分析和免疫酶学分析测定,抗体特异识别β链N-末端糖化的血红蛋白最后4~8个氨基酸组成的抗原表位。异常的血红蛋白或翻译后经修饰的血红蛋白无干扰。
目前的免疫化学试验不仅检测HbA1c,通常也同时检测HbA2c,因为血红蛋白A2糖化δ链的表位是相同的。抗体直接抗β-链的最后四个氨基酸的糖化表位的免疫化学试验也可用进行检测,例如HbS1c。在大多数情况下HbA2c意义不大,虽然镰刀细胞病时可以准确地测定缬氨酸β-N-氨基末端糖化程度,但它仍不能100%代表HbA1c。
5、离子层析法
离子层析法精密度高、重复性好且操作简单, 被临床广泛采用。检测原理由于血红蛋白β-链N 末端缬氨酸糖化后所带电荷不同, 在偏酸溶液中总糖化血红蛋白( GH b) 及H bA 均具有阳离子的特性, 因此经过阳离子交换层析柱时可被偏酸的缓冲液平衡过的树脂来吸附, 但二者吸附率不同, GH b正电荷较少吸附率较低, H bA 正电荷较多吸附率较高。用不同pH 的磷酸盐缓冲液可以分次洗脱出GH b 和H bA, 用KCN 可将H b转化为高铁氰化血红蛋白, 用分光光度计测定。或者得到相应的H b层析谱, 其横坐标是时间, 纵坐标是百分比。HbA1c值以百分率来表示。现在大部分都用全自动测定仪测定。
6、等电点聚集法
是测定GH b的新技术, 它是在聚丙烯酞凝胶中加人载体两性介质的薄板上形成一个由阳极到阴极逐渐增加的pH 梯度, 溶血液中各个组份将移动到各自的等电点的pH 位置上, 这样就得到比一般电泳法更好的分划效果和比较集中的色带, 通过分辨率高的微量光密度仪扫描, 可以准确地测定出各自组份的含量。由于它能够分辨出一级结构不同的HbA、HbAc、HbF、HbS 及HbC等, 可完全避开各种物质的干扰。
7、化学发光法
采用离子捕捉免疫分析法, 应用抗原抗体反应原理, 联以荧光标记物, 通过连接带负电的多阴离子复合物, 吸附到带正电的纤维表面, 经过一系列彻底清洗等步骤后, 测定荧光强度变化率, 计算浓度。采用专用试剂包和免疫发光分析仪,其检测系统易于规范和重复, 可减少操作技术误差, 检测的灵敏度和特异性高, 批内、批间变异系数小, 回收率高, 准确度高, 交叉污染率小, 影响因素少。
8、酶法
原理为用特殊蛋白酶分解Hb, 3~ 5 min内果糖基氨基酸从H b分离, 果糖基氨基酸氧化酶( FAOD )从果糖基氨基酸产生H2O2, H2O2经POD与DA- 64反应, 选择751 nm 测吸光度改变求得GHb浓度。
操作方案
1、操作方法 (1)收集静脉血、加入EDTA抗凝。(2)根据样品数取试管若干,分别吸取400μl溶血剂加入各试管中。(3)分别吸取80μl标准或样本放入上述各试管中,混合均匀。(4)放置5~10min,则制成了血红蛋白样本A3。
 血样
血样 2、糖化血红蛋白的制备及测定 (1)根据样品的数量,取干净的试管若干,分别吸取3.0ml阳离子树脂,放入各管中。(2)向上述试管中分别加入已预备的100μl血红蛋白样本(A3)。将层析柱插入试管中,使得橡皮塞高于液面至少1cm。(3)充分摇荡试管混合5~10min(最好使用涡旋摇荡器,如果没有则需剧烈摇荡20min。(4)然后慢慢推动层析柱进入试管,直到糖化血红蛋白提取完全。(5)上清液倒入另一支试管或直接倒入比色杯进行比色。(6)以蒸馏水作空白在415nm调零。(7)读取并记录标准,样品吸光度值。
3、总血红蛋白测定 (1)根据样品数量取试管若干,分别加入5.0ml蒸馏水。(2)加入20μl血红蛋白样本(A3)。混合均匀。(3)以蒸馏水作空白在415nm调零。(4)读取并记录各管吸光度值。
计算:糖化血红蛋白吸光度 总血红蛋白吸光度×10=糖化血红蛋白%(正常值范围6.0%~8%)。
监测意义
糖化血红蛋白的特点决定了它在糖尿病监测中有很大的意义:(1)与血糖值相平行。血糖越高,糖化血红蛋白就越高,所以能反映血糖控制水平。(2)生成缓慢。由于血糖是不断波动的,每次抽血只能反映当时的血糖水平,而糖化血红蛋白则是逐渐生成的,短暂的血糖升高不会引起糖化血红蛋白的升高;反过来,短暂的血糖降低也不会造成糖化血红蛋白的下降。由于吃饭不影响其测定,故可以在餐后进行测定。(3)一旦生成就不易分解。糖化血红蛋白相当稳定,不易分解,所以它虽然不能反映短期内的血糖波动,却能很好地反映较长时间的血糖控制程度,糖化血红蛋白能反映采血前2个月之内的平均血糖水平。(4)较少受血红蛋白水平的影响。糖化血红蛋白是指其在总血红蛋白中的比例,所以不受血红蛋白水平的影响。
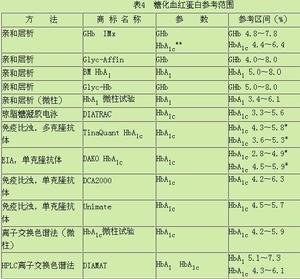 数据表
数据表 控制标准
糖化血红蛋白能够反映过去2~3个月血糖控制的平均水平,它不受偶尔一次血糖升高或降低的影响,因此对糖化血红蛋白进行测定,可以比较全面地了解过去一段时间的血糖控制水平。世界权威机构对于糖化血红蛋白有着明确的控制指标,ADA(美国糖尿病学会)建议糖化血红蛋白控制在小于7%,IDF(国际糖尿病联盟)建议糖化血红蛋白控制标准为小于6.5%,目前我国将糖尿病患者糖化血红蛋白的控制标准定为6.5%以下。
 糖化血红蛋白数据表
糖化血红蛋白数据表 糖化血红蛋白与血糖的控制情况 4%~6%:血糖控制正常。
6%~7%:血糖控制比较理想。
7%~8%:血糖控制一般。
8%~9%:控制不理想,需加强血糖控制,多注意饮食结构及运动,并在医生指导下调整治疗方案。
>9%:血糖控制很差,是慢性并发症发生发展的危险因素,可能引发糖尿病性肾病、动脉硬化、白内障等并发症,并有可能出现酮症酸中毒等急性合并症。
美国糖尿病协会(ADA),欧洲糖尿病协会(EASD)以及国际糖尿病联合会(IDF)现已达成共识,未来糖化血红蛋白的单位将采用国际临床化学联合会(International Federation of Clinical Chemistry, IFCC)标准。单位的转换可使用以下公式:
IFCC-HbA1c (毫摩尔/摩尔) = [DCCT-HbA1c (%) - 2.15] × 10.929
DCCT- HbA1c | IFCC-HbA1c |
(%) | (毫摩尔/摩尔) |
4.0 | 20 |
5.0 | 31 |
6.0 | 42 |
6.5 | 48 |
7.0 | 53 |
7.5 | 59 |
8.0 | 64 |
9.0 | 75 |
10.0 | 86 |
结果解释
实验室的检测结果可能因分析手段、样品保存时间和个体差异而不同。两个平均血糖相同的人,糖化血红蛋白可能会有多至3%的差异。结果也可能因多种因素而不可靠,如:手术后失血,输血,贫血,高红细胞更新率,慢性肾功能衰竭,肝脏疾病,高剂量维生素C摄入,红细胞生成素治疗等等。大致来说,健康人糖化血红蛋白的参考范围大约是4%–5.9%。糖化血红蛋白水平与估计的平均血糖水平的对应关系可由以下的近似公式得出:
估计的平均血糖(毫克/分升) = 28.7 × 糖化血红蛋白 − 46.7
估计的平均血糖(毫摩尔/升) = 1.59 × 糖化血红蛋白 − 2.59
(表格中的数据置信区间为95%):
糖化血红蛋白 | 估计的平均血糖 | |
(%) | (毫摩尔/升) | (毫克/分升) |
5 | 5.4 (4.2–6.7) | 97 (76–120) |
6 | 7.0 (5.5–8.5) | 126 (100–152) |
7 | 8.6 (6.8–10.3) | 154 (123–185) |
8 | 10.2 (8.1–12.1) | 183 (147–217) |
9 | 11.8 (9.4–13.9) | 212 (170–249) |
10 | 13.4 (10.7–15.7) | 240 (193–282) |
11 | 14.9 (12.0–17.5) | 269 (217–314) |
12 | 16.5 (13.3–19.3) | 298 (240–347) |
尽管高糖化血红蛋白水平代表着血糖控制不佳,但即便是"好的"糖化血红蛋白水平仍可能为段时间内的低血糖导致。因此,常规的血糖监测仍然是最佳的血糖控制分析方法。
由于糖尿病患者糖化血红蛋白的水平与平均血糖的控制相关,国际糖尿病病联合会(IDF)建议大多数糖尿病患者将糖化血红蛋白控制在6.5%以下,而美国糖尿病协会(ADA)的推荐标准则是7.0%以下。最近一些研究结果认为7%以下的控制目标过于严格,可能导致比较严重的低血糖发生。因此医疗人员在制定糖化血红蛋白控制目标时,必须考虑患者个人的健康状况、低血糖风险、特殊健康风险等具体情况。例如,对于青少年和儿童1型糖尿病患者,糖化血红蛋白的控制目标和成人有所不同,因为这部分人群血糖多变不易控制,而且在发育中的大脑比成年人的大脑更容易受到低血糖的损害,所以血糖控制不宜过分严格,美国糖尿病协会(ADA)给出的建议可参考下表:
不同年龄段青少年儿童控制目标 | |
年龄 | 糖化血红蛋白(HbA1c)控制目标 |
<6岁 | 7.5%-8.5% |
6~12岁 | <8.0% |
13~19岁 | <7.5% |
注意事项
发现治疗中存在的问题。如果糖尿病患者经常监测血糖都显示控制较好,而糖化血红蛋白偏高,则需考虑是否平时监测血糖不够全面(如只测空腹血糖而忽略了餐后血糖),或者可能血糖仪测出的数值不够准确(如机器老化,试纸受潮、过期等)。
如果某位糖尿病患者血糖波动较大,经常发生低血糖,继而又发生高血糖,由于糖化血红蛋白是反应血糖的平均值,所以其糖化血红蛋白完全有可能维持在正常范围。在这种情况下,它的数值就不能反映真正的血糖变化了。同时,糖化血红蛋白还受红细胞的影响,在合并影响红细胞质和量的疾病(如肾脏疾病、溶血性贫血等)时,所测得的糖化血红蛋白也不能反映真正的血糖水平。
指导治疗方案的调整。在临床治疗中,如能同时测定血糖与糖化血红蛋白,可以更好地全面判断病情,及时调整治疗方案。当空腹血糖超过患者糖化血红蛋白对应的预测值时,则显示近期血糖控制不好,可能与采血时紧张、劳累、晚餐进食过多、治疗不当、急性并发症等有关,需要调整治疗方案。比如某糖尿病患者定期监测糖化血红蛋白均在6%~7%,而最近一次为8.2%,这表明以往的治疗方案已不能较好地控制血糖,需要重新调整方案。相反,如果空腹血糖低于糖化血红蛋白对应的预测值,甚至达到正常标准,则显示近期血糖控制良好,治疗对症。
因此,普及糖尿病知识,更新治疗理念,监测并保持糖化血红蛋白达标,更早、更合理地使用胰岛素等药物治疗,对于控制糖尿病并发症的发生发展尤为重要。目前临床提倡对2型糖尿病患者采取积极治疗方法:尽早药物治疗、尽早联合治疗。糖尿病患者血糖控制未达到目标或治疗方案调整后,应每3个月检查一次糖化血红蛋白;血糖控制达到目标后也应每年至少检查2次糖化血红蛋白。
临床意义
临床上,只有30%左右的糖尿病患者能做到定期监测糖化血红蛋白。良好的血糖控制是预防并发症的关键,而血糖监测在很大程度上取决于患者本人的认知和行动。由于大部分患者选择可靠性不高的日常监测手段,目前超过60%的2型糖尿病患者的糖化血红蛋白控制不理想。糖化血红蛋白长期控制不稳定的影响是多方面的,它会改变红细胞对氧的亲和力,加速心脑血管并发症的形成;如果眼睛内的晶体被糖化,则会引发白内障。此外,它可引起肾小球基底膜增厚,诱发糖尿病肾病,并引起血脂和血粘度增高。糖化血红蛋白升高,是心肌梗死、脑卒中死亡的一个高危因素。在男性患者中,糖化血红蛋白每增加1%,死亡率的相对危险性增加24%,女性患者增加28%。一旦糖化血红蛋白超过7%,发生心脑血管疾病的危险性就增加50%以上。
 糖化血红蛋白仪
糖化血红蛋白仪 糖尿病患者的糖化血红蛋白控制水平没有阈值,随着糖化血红蛋白水平的降低,越接近正常值,糖尿病的并发症降低越明显,DCCT、UKPDS等国际大规模临床试验得出结论,证实糖尿病患者经强化治疗后糖化血红蛋白水平可以显著降低,各种并发症风险也明显减少。英国前瞻性研究证实糖化血红蛋白每下降1%,糖尿病相关的死亡率降低21%;心肌梗死发生率下降14%;脑卒中发生率下降12%;微血管病变发生率下降37%;白内障摘除术下降19%;周围血管疾病导致的截肢或死亡率下降43%;心力衰竭发生率下降16%。因此,糖化血红蛋白对糖尿病患者来说是一项非常重要的监测指标,它的高低直接决定将来各种严重影响糖尿病患者生活质量的慢性并发症的发生和发展。糖尿病患者定期监测糖化血红蛋白具有非常重要的意义,有助于帮助患者改善血糖控制水平,促进患者的血糖达标,从而减少并发症的发病率,从根本上改善糖尿病患者的生活质量。
糖化血红蛋白增高对人体的影响是多方面的,它可改变红细胞对氧的亲和力,使组织与细胞缺氧,加速心脑血管并发症的形成;可引起肾小球增厚,诱发糖尿病肾病(DN);还可引起血脂和血粘滞度增高,是心血管病发生的重要因素。因此,监测糖化血红蛋白不论对糖尿病患者疾病控制情况,并发症的预测情况,还是糖尿病病人的筛选等方面都有重要的意义。美国1型糖尿病控制及并发症试验(DCCT)和英国2型糖尿病控制与并发症(UKPDS)均把糖化血红蛋白作为糖尿病的一个重要评价指南,且都充分肯定了强化治疗在阻止血管并发症发生、发展的重要作用。
1 是糖尿病患者血糖总体控制情况的指标
2 有助于糖尿病慢性并发症的认识
3 指导对血糖的调整
4 对判断糖尿病的不同阶段有一定的意义
5 区别应激性血糖增高和妊娠糖尿病(GDM)中的检测意义
综上,糖化血红蛋白的检测对糖尿病患者的整体情况有很重要的意义。临床医务工作者不能仅局限在对血糖的认识上来管理血糖,应综合糖化血红蛋白才能更好的控制血糖,预防并发症的发生。美国糖尿病协会(ADA)建议血糖控制满意且稳定的糖尿病患者至少1年测2次糖化血红蛋白;若血糖控制不满意且需调整方案者,应一年测4次。另外计划怀孕的糖尿病妇女,初期每月测一次糖化血红蛋白,血糖控制满意后,应每6~8周测1次,直到受孕。同时还应该注意各种贫血,出血性疾病,或用心得安、吗飞、双氢克脲塞等药物可使糖化血红蛋白下降,而用大量阿司匹林、维生素c肾功不全,甲亢者可使其增高。应综合考虑,做到全面衡量患者的整体情况。但糖化血红蛋白不能作为诊断糖尿病的依据,也不能取代糖耐量试验,可作为糖尿病的普查和健康检查的项目。
此外还要注意 ①对昏迷病人的鉴别:在脑血管急症时,由于应激反应可使血糖增高,但糖化血红蛋白检测正常。若糖化血红蛋白增高预示患者处于高血糖状态。②糖化血红蛋白很高的患者要警惕酮症酸中毒的发生。③对妊娠糖尿病仅测定血糖是不够的,一定要监测糖化血红蛋白,并使其保持在8%以下。如此可避免巨大胎儿、死胎和畸形胎儿的发生。④指导治疗:如已测定了某病人的糖化血红蛋白,可推算出平均血糖的水平,再用推算值与同一标本的空腹血糖值对比,可预测出近期血糖控制的好坏。糖化血红蛋白小于7.3%时,餐后血糖对糖化血红蛋白的水平影响较大;当在7.3%-8.4%时,空腹和餐后血糖对糖化血红蛋白的功效差不多;当大于8.5%时空腹血糖所扮演的角色更重要。因此,糖化血红蛋白水平很高者需要更好的控制空腹血糖水平。所以,糖化血红蛋白在7%-8%者要更多干预餐后血糖,减少低血糖反应;大于8%者要兼顾空腹和餐后血糖,小于8%侧重改善餐后血糖。如若空腹血糖高于7.1mmol/L许多,糖化血红蛋白大于8%,表示近期血糖控制不好,需调整治疗方案。反之,若空腹血糖低于7.1mmol/L,甚至正常,糖化血红蛋白小于8%,则表示近期血糖控制良好,本着"效不更方"的原则,治疗方案不变。因此,同时测定血糖与糖化血红蛋白可以更好地全面判断病情,指导治疗。
标准化检测
1.HbA1c检测结果应当在全世界范围内进行标准化,包括参考系统和结果报告。
2.新的IFCC参考系统是进行A1c检测标准化的唯一有效的参考标准。
3.全世界范围,A1c报告结果必须采用IFCC单位(mmol/mol),美国国家糖化血红蛋白标准化计划(NGSP)的单位(%)必须采用IFCC-NGSP换算公式进行计算。
4.如果正在进行的"平均血糖研究"得出了优先-特异的标准,那么由A1c检测结果计算而得的A1c平均血糖(A1c Derived Average Glucose,ADAG)值应该作为A1c结果的一部分一并报告。
5.在指导临床治疗方面,血糖值和ADAG应该以IFCC单位及测得的NGSP单位表示。