溶液配制
c=n/v (mol/L)
台秤(或天平)、药匙、烧杯、玻璃棒、量筒(或量杯)、容量瓶(细口瓶)、移液管、胶头滴管 、表面皿。
- 中文名 溶液配制
- 外文名 Solution preparation
- 公式 c=n/v (mol/L)
- 常用仪器 台秤(或天平)、吸管等
- 常用固体 NaCl,NaOH。
理论
c=n/v (mol/L)
药品
固体
NaCl,NaOH。
液体
95%(ml/ml) 医用酒精、浓HCl、蒸馏水 、氯化钠 。
步骤
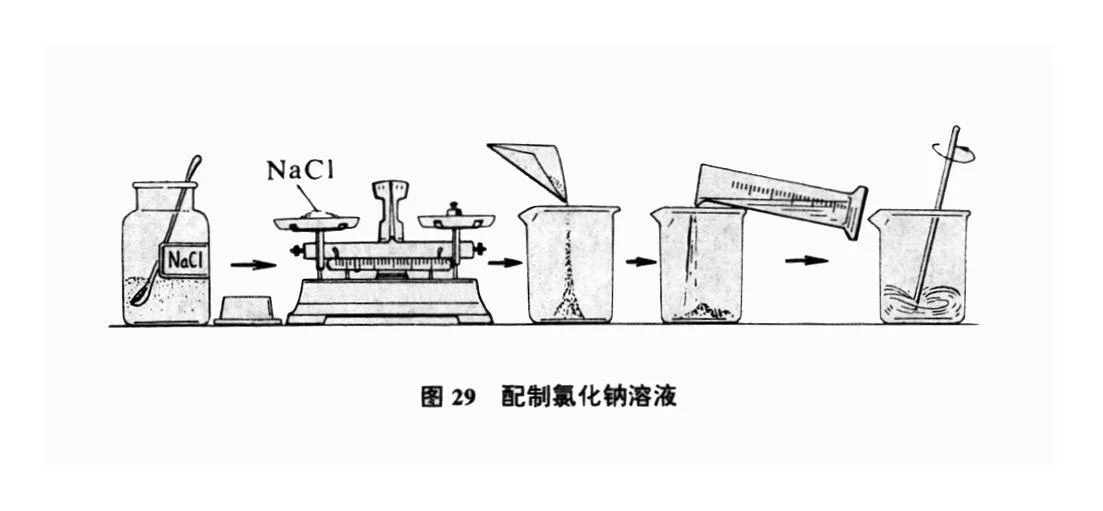
(1)计算:计算配制所需固体溶质的质量或液体浓溶液的体积。
(2)称量:用托盘天平称量固体质量或用量筒(应用移液管,但中学阶段一般用量筒)量取液体体积。
(3)溶解:在烧杯中溶解或稀释溶质,恢复至室温(如不能完全溶解可适 当加热)。检查容量瓶是否漏水
(4)转移:将烧杯内冷却后的溶液沿玻璃棒小心转入一定体积的容量瓶中(玻璃棒下端应靠在容量瓶刻度线以下)。
(5)洗涤:用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液转入容器中,振荡,使溶液混合均匀。
(6)定容:向容量瓶中加水至刻度线以下1cm~2cm处时,改用胶头滴管加水,使溶液凹面恰好与刻度线相切。
(7)摇匀:盖好瓶塞,用食指顶住瓶塞,另一只手的手指托住瓶底,反复上下颠倒,使溶液混合均匀。
最后将配制好的溶液倒入试剂瓶中,贴好标签。
误差
1.称量时引起误差。
2.未将烧杯洗涤,使溶液的物质量减少,导致溶液浓度降低。
3.转移时不小心溅出溶液,导致浓度偏低。
注意
1.氢氧化钠为碱性化学物质,浓盐酸为酸性化学物质,注意不要溅到手上、身上、以免腐蚀!
2.要注意计算的准确性。
3.注意移液管的使用。
4.稀释浓硫酸是把酸加入水中,用玻璃棒搅拌。
5.容量瓶在使用前必须检漏,检漏的步骤为注入自来水至标线附近,盖好瓶塞.右手托住瓶底,倒立2min,观察瓶塞是否渗水。如不漏,将塞子旋转180度,再检漏.如漏水,需换一套容量瓶,再检漏。
6.在配置由浓液体稀释而来的溶液时,如由浓硫酸配置稀硫酸时,不应该洗涤用来称量浓硫酸的量筒,因为量筒在设计的时候已经考虑到了有剩余液体的现象,以免造成溶液物质的量的大小发生变化!
7.移液前应静置至溶液温度恢复到室温(如氢氧化钠固体溶于水放热,浓硫酸稀释放热,硝酸铵固体溶于水吸热),以免造成容量瓶的热胀冷缩!