组蛋白是染色体基本结构蛋白,因富含硷性胺基酸Arg 和lys 而呈硷性,可与酸性的DNA紧密结合。组蛋白包含五个组分,分子质量为11-23ku,按照分子量由大到小分别称为H1、H3、H2A、H2B和H4。
组蛋白(histones)真核生物体细胞染色质中的硷性蛋白质,含精氨酸和赖氨酸等硷性胺基酸特别多,二者加起来约为所有胺基酸残基的1/4。组蛋白与带负电荷的双螺旋DNA结合成DNA-组蛋白複合物。因胺基酸成分和分子量不同,主要分成5类。组蛋白是真核生物染色体的基本结构蛋白,是一类小分子硷性蛋白质,有六种类型:H1、H2A、H2B、H3、H4及古细菌组蛋白,它们富含带正电荷的硷性胺基酸,能够同DNA中带负电荷的磷酸基团相互作用。与DNA大沟结合。
基本介绍
- 中文名:组蛋白
- 外文名:histones
- 存在:真核生物的细胞核中
- 本质:与DNA结合存在的硷性蛋白质总称
- 分子量:10000~20000
- 成分:精氨酸和赖氨酸等
简介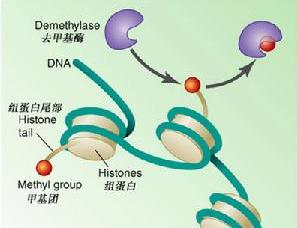 组蛋白
组蛋白
 组蛋白
组蛋白组蛋白(histone)是指所有真核生物的细胞核中,与DNA结合存在的硷性蛋白质的总称。其分子量约10000~20000。
真核生物体细胞染色质中的硷性蛋白质,含精氨酸和赖氨酸等硷性胺基酸特别多,二者加起来约为所有胺基酸残基的1/4。组蛋白与带负电荷的双螺旋DNA结合成DNA-组蛋白複合物。因胺基酸成分和分子量不同,主要分成5类。
组蛋白的甲基化修饰主要是由一类含有SET结构域的蛋白来执行的,组蛋白甲基化修饰参与异染色质形成、基因印记、X染色体失活和转录调控等多种主要生理功能,组蛋白的修饰作用是表观遗传学研究的一个重要领域。组蛋白甲基化的异常与肿瘤发生等多种人类疾病相关,可以特异性地激活或者抑制基因的转录活性。研究发现,组蛋白甲基转移酶的作用对象不仅仅限于组蛋白,某些非组蛋白也可以被组蛋白甲基转移酶甲基化,这将为探明细胞内部基因转录、信号转导、甚至个体的发育和分化机制提供更广阔的空间。
概述
组蛋白的基因非常保守。亲缘关係较远的种属中,四种组蛋白(H2A、H2B、H3、H4)胺基酸序列都非常相似,如海胆组织H3的胺基酸序列与来自小牛胸腺的H3的胺基酸序列间只有一个胺基酸的差异,小牛胸腺的H3的胺基酸序列与豌豆的H3也只有4个胺基酸不同。不同生物的H1序列变化较大,在某些组织中,H1被特殊的组蛋白所取代。如成熟的鱼类和鸟类的红细胞中H1则被H5所取代,精细胞中则由精蛋白代替组蛋白。染色质中的组蛋白与DNA的含量之比为1:1。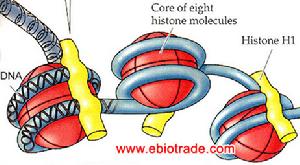 组蛋白
组蛋白
 组蛋白
组蛋白真核生物细胞核中组蛋白的含量约为每克DNA 1克,大部分真核生物中有5种组蛋白,两栖类、鱼类和鸟类还有H5以替代或补充H1。染色质是由许多核小体组成的,H2A,H2B,H3和H4各2个分子构成的8聚体是核小体的核心部分,H1的作用是与线形 DNA结合以帮助后者形成高级结构。组蛋白是已知蛋白质中最保守的,例如,人类和豌豆的H4胺基酸序列只有两个不同,人类和酵母的H4胺基酸序列也只有8个不同,这说明H4的胺基酸序列在约10^9年间几乎是恆定的。早在1888年德国化学家科塞(A.Kossel)已从细胞核中分离出组蛋白,并认识到它们作为硷性物质应在核中与核酸结合,但直到1974年才了解组蛋白的确切作用。一些实验室随后证明组蛋白以独特的方式构成核小体的组分。
组成部分
组蛋白是存在于染色体内的与DNA结合的硷性蛋白质,染色体中组蛋白以外的蛋白质成分称非组蛋白。绝大部分非组蛋白呈酸性,因此也称酸性蛋白质或剩余蛋白质。组蛋白于1834年由德国科学家A.科塞尔发现。组蛋白对染色体的结构起重要的作用。染色体是由重複单位──核小体组成。每一核小体包括一个核心8聚体(由4种核心组蛋白H2A、H2B、H3和H4的各两个单体组成);长度约为200个硷基对的脱氧核糖核酸(DNA);和一个单体组蛋白H1。长度为147硷基对的DNA盘绕于核心8聚体外面。在核心8聚体之间则由长度约为60个硷基对的DNA连线。这种DNA称为“接头”DNA。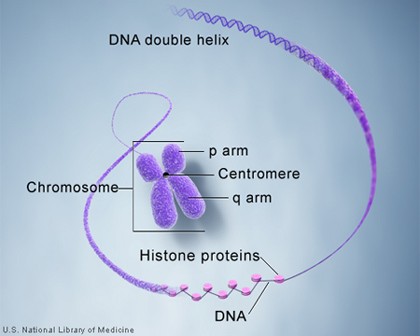 组蛋白
组蛋白
 组蛋白
组蛋白几乎所有真核细胞染色体的组蛋白均可分成5种主要的组分,分别用字母或数字命名,命名方法也不统一,如H1或称F1,Ⅰ;H2A或称F2A2,Ⅱb1;H2B或称F2B,Ⅱb2;H3或称F3,Ⅲ;H4或称F2A1,Ⅳ。有核的红细胞或个别生物体中,还存在特别的组蛋白成分,红细胞中为H5或F2C,Ⅴ,鲑鱼组织中为H6或T。H2A、H2B、H3、H4组成核小体的核心,也称核心组蛋白。根据组蛋白的一级结构,又可将它们分为3种类型:赖氨酸含量特别丰富的组蛋白(H1);赖氨酸含量较丰富的组蛋白(H2A和H2B);精氨酸含量丰富的组蛋白(H3和H4)。从整体来说,组蛋白在进化过程中保守性很强。其中H1变化较大,H3和H4变化最小。如对小牛胸腺的5种组蛋白,豌豆苗组蛋白的H3、H4和兔胸腺组蛋白H1等的一级结构比较中发现,小牛胸腺和豌豆苗的组蛋白H4间只在60位和77位上的两个胺基酸残基不同。但已知的真菌和原生动物的组蛋白的部分一级结构和动、植物的组蛋白间的差异较大。
合成修饰
这是形成组蛋白各组分微不均一性的主要原因。修饰的方式有:
①乙醯化。有两种:
一种是H1、H2A、H4组蛋白的氨基末端乙醯化,形成α-乙醯丝氨酸,组蛋白在细胞质内合成后输入细胞核之前发生这一修饰。
另一种是在H2A、H2B、H3、H4的氨基末端区域的某些专一位置形成N6-乙醯赖氨酸。
②磷酸化。所有组蛋白的组分均能磷酸化,在细胞分裂期间,H1的1~3个丝氨酸可以磷酸化。而在有丝分裂时期,H1有3~6个丝氨酸或苏氨酸发生磷酸化,其他四个核心组蛋白的磷酸化可以发生在氨基末端区域的丝氨酸残基上。组蛋白的磷酸化可能会改变组蛋白与DNA的结合。
③甲基化。仅发现于H3的9和27位和H4的20位的赖氨酸,鸭红细胞组蛋白H1和H5的组氨酸。
④ADP-核糖基化。组蛋白H1、H2A、H2B及H3和多聚ADP-核糖的共价结合,ADP-核糖基化被认为是在真核细胞内启动複製过程的扳机。
⑤其他修饰:赖氨酸的丙醯化、丁醯化、琥珀醯化、巴豆醯化、丙二酸醯等。
H3·H4的乙醯化可打开一个开放的染色质结构,增加基因的表达。转录共同激活物如CBPöP300、PCAF实质上是体内的组蛋白乙醯基转移酶(HAT)。相反,HDAC参与组成转录共同抑制複合物,已发现的两个共同抑制複合物SIN3、Mi22NHRD(核小体重塑蛋白去乙醯基酶)都含有HDAC1、HDAC2。SIN3的组成为核心(HDAC1、HDAC2、RBAP46öRBAP48)SIN3AöSIN3B、SAP30öSAP18共同构成。
SIN3複合物通过组分SIN3A与序列特异性转录因子或共同抑制物包括mael2max,核激素受体N2CORöSMRT、甲基化CPG粘附蛋白(MECP2、MBD2)相互作用。Mi22NHRD由核心(HDAC1、HDAC2、RBAP46öRBAP48)Mi2、MTA1öMTA2、MBD3组成,其中MBD3含有MBD样序列,与甲基化DNA有低亲和力,分析发现MBD3与甲基化有关的胺基酸被置换,由此推测MBD3与MBD2相互作用而使Mi22NURD与甲基化DNA结合。由此看出,DNA甲基化和组蛋白去乙醯化协同作用共同参与转录阻遏。
此外,Mi22NURD还有染色质重塑活性,所以SIN3和Mi22NURD可能分别在长期和短期转录阻遏调节中起作用。
在哺乳动物基因组中,组蛋白则可以有很多修饰形式.一个核小体由两个H2A,两个H2B,两个H3,两个H4组成的八聚体和147bp缠绕在外面的DNA组成.组成核小体的组蛋白的核心部分状态大致是均一的,游离在外的N-端则可以受到各种各样的修饰,包括组蛋白末端的乙醯化,甲基化,磷酸化,泛素化等等。
组蛋白被甲基化的位点是赖氨酸和精氨酸.赖氨酸可以分别被一、二、三甲基化,精氨酸只能被一、二甲基化.在组蛋白H3上,共有5个赖氨酸位点可以被甲基化修饰。
一般来说,组蛋白H3K4的甲基化主要聚集在活跃转录的启动子区域。组蛋白H3K9的甲基化同基因的转录抑制及异染色质有关。EZH2可以甲基化H3K27,导致相关基因的沉默,并且与X-Chromosomeinactivation相关。H3K36的甲基化同基因转录激活相关。
成分
通常含有H1,H2A,H2B,H3,H4等5种成分。除H1外,其他4种组蛋白均分别以二聚体(共八聚体)相结合,形成核小体核心。DNA便缠绕在核小体的核心上。而H1则与核小体间的DNA结合。因此,一般认为组蛋白作为结构支持体的作用比其基因调节作用更为重要。鸟类、两栖类等含有细胞核的红细胞中,含有一种叫H5的特殊组蛋白。此外,在停止增殖的细胞中,还含有一种叫H1°的组蛋白,H1°的结构与H5相类似。组蛋白可受到甲基化、乙醯化、磷酸化、聚ADP核糖醯化,以及与泛醌(ubiquinone)相结合等几种类型的修饰。组蛋白的修饰与染色质结构的变化及基因活性控制的相关性等等,是今后的重要研究课题。
分类特徵
种类 | 赖氨酸/精氨酸 | 残基数 | 分子质量(kd) | 保守性 | 存在部位及结构作用 |
H1 | 29.0 | 215 | 23.0 | 低 | 连线线上,锁定核小体、参与包装 |
H2A | 1.22 | 129 | 14.0 | 高 | 核心颗粒,形成核小体 |
H2B | 2.66 | 125 | 13.8 | 高 | 核心颗粒,形成核小体 |
H3 | 0.77 | 135 | 15.3 | 极高 | 核心颗粒,形成核小体 |
H4 | 0.79 | 102 | 11.3 | 极高 | 核心颗粒,形成核小体 |
H1富含硷性胺基酸
医学套用
预测
最新研究结果显示:组蛋白修饰的整体模式可预测低分级前列腺癌的复发风险。该研究第一作者加利福尼亚大学的Siavash K. Kurdistani表示:这种修饰模式最终可作为前列腺或其他类型癌症的预后或诊断指标,也可作为预测何种患者、患者会对一类o组蛋白去乙醯酶抑制剂新药产生反应的指标。Kurdistani解释:某些组蛋白修饰模式会在一定水平上影响基因的表达,但具体机制尚不清楚。
Kurdistani等人研究了五种组蛋白修饰模式,包括3种乙醯化作用,2种二甲基化作用,用组织晶片技术对原发前列腺癌组织样品中的组蛋白修饰水平进行检测。
研究者对104例Gleason评分小于7的样本进行染色组蛋白修饰检测,结果将研究对象分为2组,第1组10年内复发危险为17%,第2组为42%。该预测指标与肿瘤分期,术前PSA水平或是否包膜外侵犯相独立。
研究者对另外的39例低分级前列腺癌样本的组蛋白修饰模式进行了确认,结果也分为2组,1组的复发危险为4%,另1组为31%。
研究者最后表示:考虑到组蛋白修饰模式的多样性,其他组蛋白修饰位点的信息将有助于我们对患者进行进一步分类,包括那些高分极组的患者。套用免疫组化及越来越多的的抗体检测组蛋白修饰将有助于这种检测指标在其他肿瘤中的套用。
调控
组蛋白修饰与基因表达调控有关已经被广泛的证明了。PierreEtchegary,StevenReppertandcoworkers的研究表明组蛋白修饰,特别是组蛋白乙醯化对于哺乳动物生物钟的调控是非常重要的。
调控生物钟的关键蛋白Clock和Bmal1驱动着三个period基因(Per1,2,3)和两个细胞色素基因(Cry1,2)的表达。这5个基因的转录本覆盖了生物24小时的时间。但奇怪的是Clock/Bmal1对Per启动子的结合相对稳定,而它们对Cry1启动子最强的结合却反应着Cry1表达的最弱。在这篇文章中E发现是染色体结构的修饰来决定Per和Cry基因的转录的。
研究者用甲醛交连的染色体免疫沉澱CHIP和半定量的PCR反应的方法发现在Per1和Per2的启动子上组蛋白3的乙醯化在全天都存在,而RNA多聚酶Ⅱ也一直被招募在这些启动子上。当H3被乙醯化和RNA多聚酶Ⅱ结合最强时,Per转录本水平最高,这说明H3的乙醯化可能通过促进将RNA多聚酶Ⅱ招募到启动子上而促进基因的转录。Cry基因座位的表达也有类似的相关性。
研究者发现具有蛋白质乙醯化活性的p300在小鼠肝细胞中能与Clock组成複合物。研究者认为白天p300/Bmal1/Clock结合在启动子上,促进H3乙醯化,RNA多聚酶Ⅱ招募到启动子上而Per基因发生转录。夜间p300与Bmal1/Clock进行解离,导致组蛋白的去乙醯化而抑制基因的转录。
那幺,导致p300基因日夜节律的是什幺呢?
研究者发现是Cry对其进行负调控的结果,研究者发现Cry1,2抑制p300/Bmal1/Clock驱动的基因转录。他们认为可能是Cry对p300/Bmal1/Clock複合物进行去稳定性作用而对其功能进行抑制。乙醯化对基因表达的调控已经广为人知,这个新的研究更让人们确定组蛋白的乙醯化对基因表达的调控具有很广泛的作用。